Immunità contro il cancro

ATTUALITÀ PER LA CLASSE | Biologia
Nelle prime fasi di un tumore, il sistema immunitario riesce a riconoscerlo e ad attaccarlo, ma a un certo punto questa capacità viene meno e il tumore ha la meglio. Nuove strategie terapeutiche, sempre più promettenti, puntano a potenziare il sistema immunitario per sconfiggere la malattia. Vediamo di cosa si tratta.
Il nostro sistema immunitario è molto complesso, ma il principio sul quale si basa è semplicissimo: essenzialmente, quello che fa è distinguere il sé (le nostre cellule, i nostri tessuti, i nostri organi) dall’altro (i parassiti, gli organi estranei ecc.). La domanda quindi è: dal momento che un tumore è fatto di cellule mutate geneticamente, quindi in parte diverse dalle cellule sane, l’armamentario da difesa che possediamo potrebbe riconoscere e distruggere il cancro nello stesso modo in cui riconosce ed eradica un virus dell’influenza?
L’intuizione di Ehrlich
La questione se l’era posta, oltre centro anni fa, uno dei padri dell’immunologia: Paul Ehrlich geniale microbiologo tedesco che ha coniato alcuni famosi termini che ci portiamo ancora dietro (come anticorpo e chemioterapia), ha messo a punto il primo farmaco sintetico contro la sifilide e per le sue scoperte sul sistema immunitario ha vinto nel 1908 il Premio Nobel per la medicina e la fisiologia, insieme al russo Il’ja Mečnikov. Ebbene, anche quella sua intuizione era corretta, come aveva poi provato per la prima volta un altro pioniere dell’immunologia, l’americano William Bradley Coley, nel 1898. Iniettando in pazienti malati di tumore una sorta di vaccino ottenuto con frammenti di batteri, Coley aveva scatenato una forte risposta immunitaria in grado di ridurre le masse tumorali.
Verso una nuova avventura
Ora facciamo un salto nel tempo e torniamo al 2016. È ottobre e siamo a Copenaghen, al congresso europeo di oncologia (Esmo).
Tra i molti studi presentati ce n’è qualcuno che attira parecchia attenzione. Sono sperimentazioni che stanno cambiando la vita dei pazienti con il melanoma (che colpisce anche i giovanissimi), con il cancro del polmone, del rene e della vescica: tumori per i quali non avevamo molte armi a disposizione e che ora sono stati trattati con farmaci nuovi e molto promettenti.
Li chiamano immunoterapie. Con questo termine si intendono tutti i farmaci e i prodotti biologici (come i vaccini) che mirano a stimolare il sistema immunitario affinché reagisca contro il “nemico”, invece che colpirlo direttamente. Il principio non è certo nuovo, quindi, ma in questo caso è stato applicato efficacemente alla cura dei tumori, proprio come aveva immaginato Ehrlich. Insomma, dopo anni di tentativi e studi, questo approccio sta dando dei risultati e si comincia a parlare di immuno-oncologia (cioè, per l’appunto, l’uso degli immunoterapici in oncologia).
È chiaro a tutti – ricercatori in primis – che siamo solo all’inizio di un’avventura. Nessuno sa dove porterà questa strada ed è bene ricordarlo subito: si parla di speranze, non di certezze, perché le sperimentazioni sono ancora in corso.
Quel che è sicuro è che per la medicina è comunque una rivoluzione: l’immuno-oncologia è un modo completamente nuovo di affrontare il cancro.
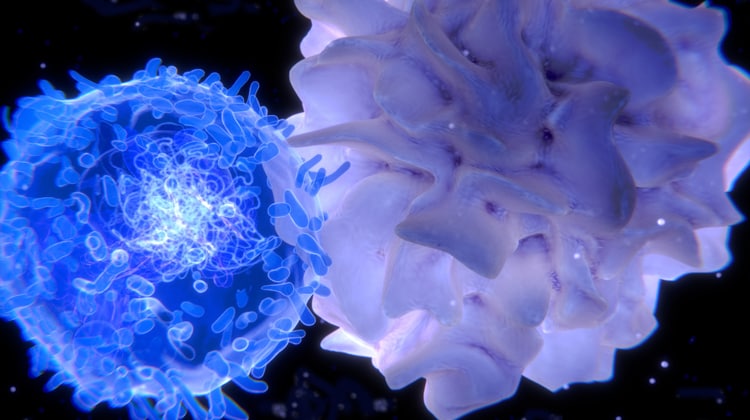
Primo (ri)conoscimento del nemico
Perché il sistema immunitario, da solo, non riesce a tenere a bada le cellule cancerose? In realtà lo fa nella maggior parte dei casi. Il fatto è che, a un certo punto, le cellule tumorali diventano molto brave ad eluderlo. «All’inizio il sistema immunitario vede le cellule tumorali come un sé modificato, diverso, e le attacca», spiega Maria Rescigno, direttrice del Programma di immunoterapia dell’Istituto europeo di oncologia (Ieo) di Milano e ricercatrice Airc (Associazione italiana per ricerca sul cancro). Ecco cosa avviene normalmente: le cellule dendritiche – un tipo di cellule del sistema immunitario, che ne rappresentano una specie di avamposto – intercettano gli antigeni presenti è qualunque molecola capace di stimolare una reazione immunitaria e nel caso specifico gli antigeni tumorali altro non sono che proteine mutate presenti sulla superficie del tumore, e perciò diverse da quelle che si trovano sulle cellule sane. Dopo averlo intercettato, le cellule dendritiche inglobano l’antigene al loro interno e migrano nei linfonodi dove passano l’informazione su come riconoscere questo nemico ai linfociti T citotossici (i killer del nostro sistema immunitario), che dovranno svolgere il “lavoro sporco”. Allertati e istruiti, infatti, i linfociti T killer si moltiplicano e vanno alla ricerca di quello stesso antigene. Una volta individuato vi si legano e rilasciano sostanze in grado di uccidere le cellule tumorali. «Ad un certo punto però – continua Rescigno – il tumore stesso fa in modo di essere percepito come sé. In pratica, induce una tolleranza nei suoi confronti, e lo fa in almeno due modi: da una parte non espone più sulla sua superficie gli antigeni che avevano provocato la risposta iniziale, dall’altra rilascia molecole che frenano i linfociti T citotossici.» Ecco quindi la filosofia, molto semplice, sulla quale si basa l’immuno-oncologia: rieducare il sistema immunitario affinché torni a riconoscere il cancro come non sé.
I nuovi vaccini anticancro
Come si fa? Con il vecchio metodo del vaccino, realizzato però servendosi delle nuove conoscenze della genomica: «Si prende un piccolo campione di tumore asportato durante un intervento chirurgico e ne si analizza il DNA», spiega Rescigno. «Le sequenze ottenute vengono inserite in una library digitale (una sorta di catalogo) e confrontate con quelle delle cellule di individui sani. L’obiettivo è individuare le differenze nei geni che codificano per gli antigeni. A questo punto, sulla base delle porzioni mutate di DNA, si generano sinteticamente dei frammenti (peptidi) di questi antigeni e li si usa per formulare il vaccino. L’obiettivo è attivare i linfociti T citotossici in modo altamente specifico contro questi antigeni.» Ad oggi i vaccini anticancro sono in studio soprattutto per il melanoma, perché è il tumore più immunogenico (cioè, quello che più facilmente scatena una risposta immunitaria).
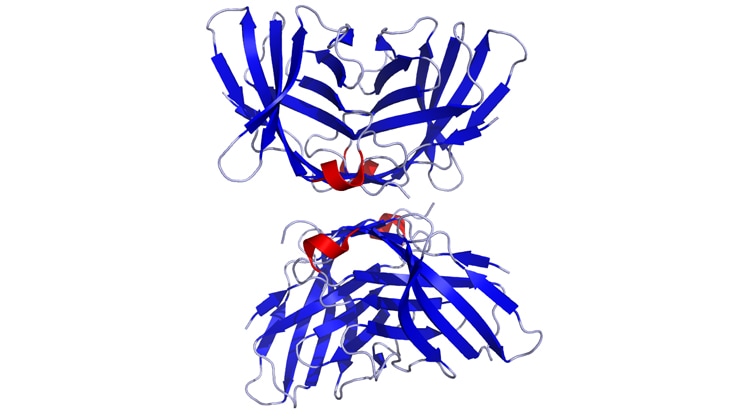
Checkpoint!
Abbiamo detto che il tumore è anche in grado di rilasciare molecole che “addormentano” il sistema immunitario. Per l’esattezza, altro non fa che sfruttare il “sistema di sicurezza” che nelle persone sane evita le risposte immunitarie quando non servono. Questo sistema di sicurezza usa proteine che si legano ai linfociti T e li “frenano”. I ricercatori le chiamano checkpoint (posti di blocco), e un’intuizione felice dell’immuno-oncologia è stata quella di provare a eliminare questi freni.
L’idea venne a Jim Allison, allora direttore del Cancer Research Laboratory dell’Università della California di Berkeley, negli anni Novanta. In un articolo pubblicato su Science nel 1996, Allison dimostrava che iniettando nei topi un anticorpo in grado di inibire l’azione del checkpoint CTLA-4 (Cytotoxic T lymphocyte-associated molecule-4), si poteva arrestare la crescita dei tumori. Non solo: l’anticorpo sembrava conferire l’immunità anche verso una successiva esposizione degli animali alle cellule tumorali. In sostanza, il sistema immunitario era tornato in grado di aggredire il cancro.
Giù il freno
Per passare dalle sperimentazioni sugli animali a un farmaco per gli esseri umani ci sono voluti circa 14 anni. Sei anni fa, infatti, il New England Journal of Medicine pubblicava il primo studio clinico sull’inibitore del CTLA-4 in pazienti con melanoma avanzato. La molecola – come spesso accade in medicina – ha un nome complicato: Ipilimumab. I risultati mostravano che questo rivoluzionario farmaco era in grado di prolungare la vita dei pazienti ma, ancora più importante, per alcuni di loro l’effetto sembrava persistere: in alcuni casi, i pazienti erano persino apparentemente guariti dal melanoma. I risultati si possono riassumere in una frase: piccoli benefici per molti, enormi benefici per pochi, in ogni caso insperati e mai osservati prima.
Ipilimumab è stato approvato dalle agenzie regolatorie americana ed europea del farmaco (Fda e Ema) per la messa in commercio nel 2011.
Da allora, altri inibitori dei checkpoint sono stati messi a punto. Il secondo si chiama pembrolizumab e sblocca un altro importante freno individuato dai ricercatori: PD-1 (Programmed cell Death-1). I nuovi dati su questo farmaco mostrano che è molto più efficace della chemioterapia nel tumore del polmone, tanto che, in alcuni casi selezionati, potrebbe sostituirla in un prossimo futuro.

I prossimi passi
Fino ad oggi sono stati condotti studi clinici sui vaccini e sugli inibitori degli immuno-checkpoint separatamente, ma il prossimo passo sarà combinare le due strategie. Soprattutto per i tumori non immunogenici, togliere i freni non basta: perché la “macchina” si muova bisogna metterla in discesa, potenziando la risposta immunitaria con i vaccini.
Non è tutto: come abbiamo visto c’è un “però” che placa l’entusiasmo. Questi farmaci innovativi non funzionano per tutti nello stesso modo, e la sfida sarà quella di capire, prima ancora di somministrarli, per quali pazienti saranno efficaci e per quali no: la nuova frontiera della medicina personalizzata. Una frontiera importare per i malati stessi, prima di tutto, ma anche per la sostenibilità del Sistema sanitario nazionale, dal momento che queste cure sono molto costose.
Macrofagi traditori
Nel microambiente in cui è immerso il tumore si trovano anche cellule sane. Alcune di queste sono macrofagi, cellule del sistema immunitario che proteggono l’organismo fagocitando microorganismi e particelle estranee. I macrofagi sono potenzialmente in grado di colpire il cancro, ma invece di svolgere il loro lavoro si comportano come poliziotti corrotti e aiutano la crescita e la diffusione delle metastasi, per esempio promuovendo la formazione di nuovi vasi sanguigni. Ancora: preparano un microambiente infiammatorio che facilita l’insediamento delle cellule neoplastiche. Vengono chiamati Tam (macrofagi associati al tumore) e da tempo si cercano strategie per colpirli. La svolta potrebbe arrivare grazie a Ecteinascidia turbinata, un piccolo invertebrato marino che produce una molecola, la trabectidina, che sembra in grado di neutralizzare i Tam.
La scoperta è frutto di una collaborazione tra diversi poli di ricerca milanesi.
PER APPROFONDIRE
- Couzin-Frankel J., Cancer Immunotherapy, in Science, 2013, vol. 342, pp. 1432-1433.
- Farrell A., Immune Surveillance, in Nature Milestones Cancer.
- Mantovani A., Immunità e vaccini, Mondadori, Milano 2016.
- Mantovani A., La promessa dell’immunoterapia, in Le Scienze, vol. 574, giugno 2016.
- Weintraub K., Come difendersi dal cancro, in Le Scienze, vol. 574, giugno 2016.
- The story of Yervoy (ipilimumab), Cancer Research Laboratory, UC Berkeley.
- Immunoncologia, opuscolo informativo a cura dell’Associazione italiana di oncologia medica.